한미약품품의 급성 골수병 백혈병 치료제 - HM43239 엡 토즈와 5000억 원 규모 L/O 계약 체결을 했다는 소식입니다.
한미약품이 급성 골수성 백혈병 (AML) 치료제 후보 불질로 5000억 원 규모의 기술 수출(L/O)에 성공했습니다. 수차레 권리 반환의 아픔을 격은 한미약품이 이번 계약으로 L.O 시장의 강자임을 다시 한번 입증했다는 분성입니다.

한미약품은 지난 4일 공시를 통해 나스닥 상장 바이오 기업 엡 토즈 바이오 사이언스와 AML 치료 신약으로 개발 중인 FLT3 억제제(HM43239)의 L/O 계약을 체결했다고 밝혔습니다.
앱 토즈는 캐나다에 본사를 둔 혈액질환 연구개발(R&D) 기업입니다. 제발, 불응성 AML, 고위험 골수 이형 형성 증후군 (MDS) 혈액종양 치료 신약 후부 물질 4개를 보유하고 있습니다. 이번 계약으로 앱 토즈는 HM43239의 전 세계 개발 및 상업화에 대한 독 전적 권리를 확보했습니다.
총 계약금액은 최대 4억 2000만 달러(약 4961억 원이라 합니다. 계약규모는 지나 해 매출 (1조 759억 원)의 46.1%에 해당합니다.
한미약품은 계약금 1250만 달러(약 148억 원)를 현금 500만 달러와 750만 달러 규모의 앱토스 주식으로 나눠 받는다고 합니다. 단계별 임상 개발, 허가 상업화 마일스톤은 최대 4억 750만 달러(약 4813억 원)입니다.
제품 상용화 후에는 순매출액의 일정 비율로 경상기술료 (로열티)를 받게 됩니다.
HM43239는 AML을 유발하는 FLT3 돌연변이와 SYK를 이중 억제하는 혁신신약입니다. 골수성 악성 종약의 증식, 분화, 내성 등의 치료 과정에 관여한다고 합니다. 지난 2018년 미국 식품의약국(FDA)으로부터 희귀 의약품(ODD)으로, 시품 의약품 안전처로부터 개발 단계 ODD로 지정되었다는 소식을 전합니다.
현제 미국에서 임상 1/2상을 진행 중입니다. 임상시험은 오는 2023년 초 마무리할 예정입니다.
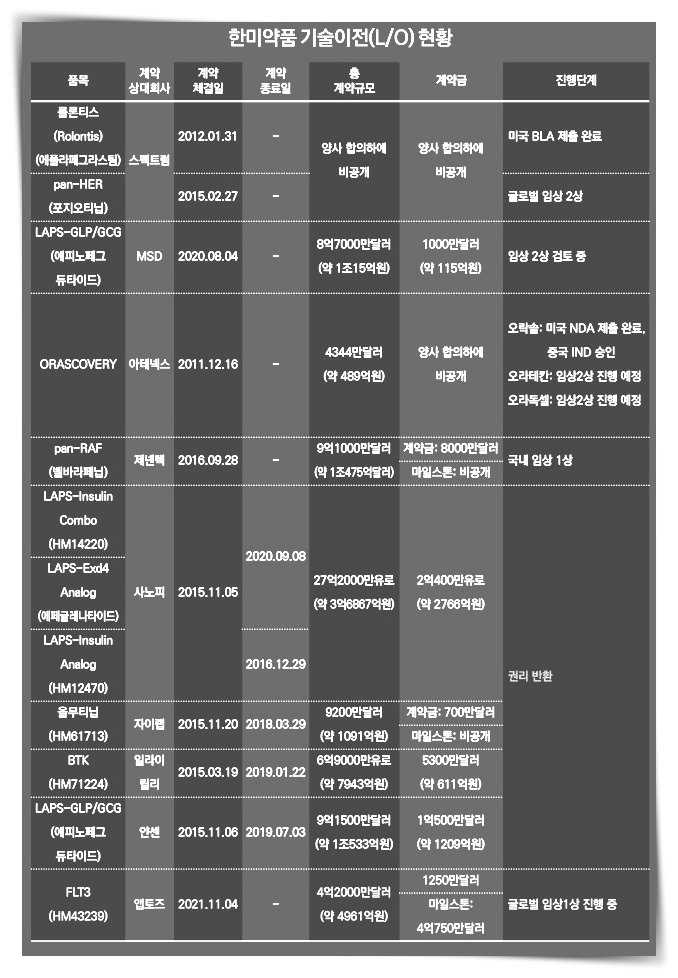
한미약 품으니 최근 대규모 L/O계약이 잇따라 취소되면서 어려움을 겪었다고 합니다.
다국 전 제약사 사노피는 지난해 당뇨병 치료 신약 후보물질 HM14220과 에페를 레나 타이드의 권리를 반환했습니다.
앞선 2019년엔 알라이릴리, 얀센과 각각 체결했던 류머티즘 관절염 치료제와 비만, 당뇨 치료제 L/O 계약이 취됐습니다. 독일 베링거 인겔하임과 중국 자이 랩에 이전했던 표적항암제 HM61713도 지난 2016년과 2018년에 권리 반환이 이뤄졌습니다.
그럼에도 한미약품은 기술 수출했던 파이프라인에서 성과를 내고 있습니다. 한미약품 파트너사인 스펙 트러은 올해 4분기 내로 항암 신약 포지오티닙의 FDA 조건부 허가를 신청할 예정입니다. 지난 8월 FDA로부터 보완요구 서한 (CRL)을 받았던 호중구감소증 치료제 롤론티스는 이르면 오는 2022년 상반기 중으로 허가신청(BLA)할 것으로 예상됩니다.
특히 이번 계약은 한미약품이 국내 L/O 시장의 선구자로서 입지를 굳혔다는 점에서 의미가 있습니다.
업계에선 그동안 글로벌 빅파마와 조 단위 L/O계약을 성사시킨 한미약품의 기술력을 다시금 입증하는 계기가 됐다고 평가한다고 합니다.
이번 HM43239 기술이전을 기점으로 한미약품의 R&D 파이프라인들에 대한 성과 재부각이 기대된다고 전문가들은 판단하고 있습니다. 포지오티닙, 벨바 라페 닙 등 기술 이전된 파이프라인들의 임상시헙도 순항 중인 만큼 주목할 필요가 있다고 판단하고 있습니다.
'기업관련 자료' 카테고리의 다른 글
| 글로벌 철강시황과 전망 알아보기. (0) | 2021.12.31 |
|---|---|
| SK스퀘어- 원스토어가 IPO 1호 타자가 된 사연은? (0) | 2021.12.02 |
| 현대자동차- 에이플러그 통째로 인수 /커넥티드카 개발 가속!!! (1) | 2021.11.27 |
| 에스맥- 하웨이 터치모듈 공급 끊겨 매출이 수직하강하다. (0) | 2021.11.03 |
| 탄소중립을 위해 기업들이 뭉치다.친환경및 재생에너지관련 /포스코/삼성엔지니어링/롯데케미칼/두산 퓨얼셀/sk에너지/현대차그룹/기아차/삼성중공업 (0) | 2021.10.31 |